-
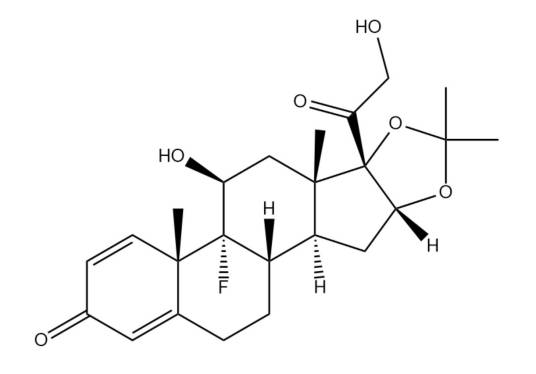
曲安奈德 编辑
中文名:曲安奈德
外文名:Triamcinolone acetonide
别名:醋酸曲安缩松;去炎舒松
化学式:C24H31FO6
分子量:434.498
CAS登录号:76-25-5
EINECS登录号:200-948-7
熔点:274 至 278 ℃
沸点:576.9 ℃
密度:1.33 g/cm³
外观:白色至灰白色结晶性粉末
闪点:302.7 ℃
安全性描述:S45;S53
危险性符号:T
危险性描述:R61
基本信息
化学式:C24H31FO6
分子量:434.498
CAS号:76-25-5
EINECS号:200-948-7
理化性质
密度:1.33g/cm3
熔点:274-278℃
沸点:576.9ºC
闪点:302.7ºC
折射率:1.589
外观:白色至灰白色结晶性粉末
分子结构数据
摩尔折射率:109.41
摩尔体积(cm3/mol):324.8
等张比容(90.2K):882.9
表面张力(dyne/cm):54.5
极化率(10 -24cm 3):43.37
计算化学数据
疏水参数计算参考值(XlogP):无
氢键供体数量:2
氢键受体数量:7
可旋转化学键数量:2
互变异构体数量:9
拓扑分子极性表面积:93.1
重原子数量:31
表面电荷:0
复杂度:925
同位素原子数量:0
确定原子立构中心数量:8
不确定原子立构中心数量:0
确定化学键立构中心数量:0
不确定化学键立构中心数量:0
共价键单元数量:1
基本信息
本品为9-氟-11β,21-二羟基-16α,17-孕甾-1,4-二烯-3,20-二酮,按干燥品计算,含C24H31FO6应为97.0%~102.0%。
性状
本品为白色或类白色结晶性粉末,无臭。
本品在丙酮中溶解,在三氯甲烷中略溶,在甲醇或乙醇中微溶,在水中极微溶解。
比旋度
取本品,精密称定,加二氧六环溶解并定量稀释制成每1mL中约含10mg的溶液,依法测定(通则0621),比旋度为+101°至+107°。
吸收系数
取本品,精密称定,加乙醇溶解并定量稀释制成每1mL中约含10μg的溶液,照紫外-可见分光光度法(通则0401),在239nm的波长处测定吸光度,吸收系数(E1%1cm)为340~370。
鉴别
1、在含量测定项下记录的色谱图中,供试品溶液主峰的保留时间应与对照品溶液主峰的保留时间一致。
2、本品的红外光吸收图谱应与对照的图谱(光谱集603图)一致。
检查
氟
取本品,依法检查(通则0805),含氟量应为4.0%~4.75%。
有关物质
照高效液相色谱法(通则0512)测定。
供试品溶液:取本品约25mg,置50mL量瓶中,加甲醇35mL,振摇使溶解,用水稀释至刻度,摇匀。
对照溶液:精密量取供试品溶液1mL,置100mL量瓶中,用70%甲醇溶液稀释至刻度,摇匀。
系统适用性溶液:取曲安奈德与曲安西龙适量,加70%甲醇溶液溶解并稀释制成每1mL中各约含5µg的溶液。
色谱条件:用十八烷基硅烷键合硅胶为填充剂,以甲醇-水(525:475)为流动相,检测波长为240nm,进样体积20μL。
系统适用性要求:系统适用性溶液色谱图中,理论板数按曲安奈德峰计算不低于5000,曲安奈德峰与曲安西龙峰的分离度应大于15。
测定法:精密量取供试品溶液与对照溶液,分别注入液相色谱仪,记录色谱图至主成分峰保留时间的3.5倍。
限度:供试品溶液色谱图中如有杂质峰,单个杂质峰面积不得大于对照溶液主峰面积的0.3倍(0.3%),各杂质峰面积的和不得大于对照溶液主峰面积0.8倍(0.8%),小于对照溶液主峰面积0.01倍的峰忽略不计。
干燥失重
取本品,在105℃干燥至恒重,减失重量不得过1.5%(通则0831)。
炽灼残渣
不得过0.2%(通则0841)。
硒
取本品0.10g,依法检查(通则0804),应符合规定(0.005%)。
含量测定
照高效液相色谱法(通则0512)测定。
供试品溶液
取本品适量,精密称定,加甲醇溶解并定量稀释制成每1mL中约含30µg的溶液。
对照品溶液
取曲安奈德对照品适量,精密称定,加甲醇溶解并定量稀释制成每1mL中约含30µg的溶液。
系统适用性溶液、色谱条件与系统适用性要求
见有关物质项下。
测定法
精密量取供试品溶液与对照品溶液,分别注入液相色谱仪,记录色谱图。按外标法以峰面积计算。
类别
肾上腺皮质激素药。
贮藏
遮光,密封保存。
制剂
1、曲安奈德注射液。
2、曲安奈德益康唑乳膏。
药理作用
曲安奈德为曲安奈德A的醋酸酯衍生物。是中效糖皮质激素。作用与曲安西龙相似,具有抗炎、抗瘙痒和收缩血管等作用,水钠潴留作用微弱,其中抗炎作用较强而持久。曲安奈德4mg的抗炎活性约相当于5mg的泼尼松龙或相当于20mg氢化可的松。曲安奈德为长效肾上腺皮质激素类药,作用机制与曲安西龙相似,具有抗炎、抗瘙痒和收缩血管的作用。其抗炎和抗过敏作用较强而持久,效力比可的松大20~30倍。曲安奈德具有抗炎、抗瘙痒和收缩血管的作用。其抗炎和抗过敏作用较强且较持久。对皮炎和其他皮肤病,可经皮肤涂擦、封闭敷裹疗法,而由皮肤吸收。曲安奈德局部使用时的耐受性极佳。
药代动力学
曲安奈德口服易吸收,口服5mg,生物利用度约23%,1h血药浓度达峰值10.5ng/mL,半衰期为2.0h;肌内注射吸收缓慢,数小时内起效,1~2天达最大效应。作用可维持2~3周;皮内、关节腔内局部注射吸收缓慢,作用持久,一般注射一次疗效可维持1~2周以上。与血浆白蛋白蛋白结合少。吸收后在肝、肾和组织中代谢为无活性代谢物,经肾脏排出。
禁忌症
1、对肾上腺皮质激素类过敏者。
2、精神病患者或有严重的精神病史。
3、活动性胃十二指肠溃疡。
4、新近胃肠吻合术后。
5、较重的骨质疏松。
6、明显的糖尿病。
8、淋球菌感染。
9、全身性真菌感染。
10、伴有感染性的活动期关节炎或皮炎。
11、酒精性肝硬化伴腹水。
12、儿童。
13、孕妇和哺乳期妇女。
用法用量
1、用于支气管哮喘:每次40mg,3周1次,连续5次为1个疗程,症状较重者每次80mg;6~12岁儿童减半,在必要时3~6岁幼儿可用成人剂量的1/3。用于过敏性鼻炎:每次40mg,每3周1次,连续5次为1个疗程,或下鼻甲注射,鼻腔先喷1%的利多卡因液表面麻醉后,在双下鼻甲前端各注入曲安奈德5~20mg,每周1次,连续5次为1个疗程。
2、关节或局部注射:
(1)用于各种骨关节病:每次2.5~20mg,溶于0.25%利多卡因10~20mL中,用5号针头,一次进针直至病灶,每周2~3次或隔日1次,症状好转后每周1~2次;每4~5次为1个疗程;
(2)用于皮肤病:直接注入皮损部位,通常每一部位用0.2~0.3mg,视患部大小而定,每处每次不超过0.5mg,必要时每隔1~2周重复使用。
3、外用:应用软膏、乳膏、滴眼剂涂敷患处,每天1~4次。气雾剂喷布,每天3~4次。外阴鳞状上皮增生:每天涂擦局部3~4次。瘙痒顽固、表面用药无效的硬化性苔藓可用曲安奈德混悬液皮下注射。
4、口服:初始一次4mg,每天2~4次,维持量每次1~4mg,每天1~2次。
5、皮下注射:每次5~25mg,每周1~2次。
注意事项
1、局部注射时,有高血压、心脏病、糖尿病、骨质疏松症、青光眼、肝肾功能不全等的患者视病情慎用乃至禁用。
2、曲安奈德在使用前应充分摇匀。使药液成一均匀悬浮液。
3、不宜用作静脉注射,局部注射时不应太浅,每次用药总量不要过多。
4、长期外用,可致耐药性。
5、对并发细菌或真菌感染的皮肤病,应与相应的抗细菌或抗真菌药合用。
6、曲安奈德潴钠作用微弱,不宜用于肾上腺皮质功能减退的替代治疗。
7、孕妇不宜长期应用。
8、曲安奈德仅作外用,避免与眼接触。
9、病毒性皮肤病者禁用。
不良反应
本品较大剂量易引起糖尿病、消化道溃疡和类柯兴综合征症状,对下丘脑-垂体-肾上腺轴抑制作用较强。并发感染为主要的不良反应。
1、长期使用大剂量的皮质激素,可以引起水、盐、糖、蛋白质及脂肪代谢紊乱:表现为向心型肥胖、满月面容、多毛、无力、低血钾、水肿、高血压、糖尿病等,临床上称之为库欣综合征。这些症状可以不做特殊治疗,停药后一般会自行逐渐消退,数月或较长时间后可恢复正常。必要时可配用降压、降糖药物,并给予低压、低糖、高蛋白饮食及补钾等对症治疗。因此,有高血压、动脉硬化、肾功能不全及糖尿病的病人,应该适当补充维生素D及钙剂,要慎重应用皮质激素。
2、诱发或加重感染:皮质激素有抗炎作用,但不具有抗菌作用,并且能降低机体抗感染能力,使机体的抗病能力下降,利于细菌生长、繁殖和扩散。因此,长期应用皮质激素可诱发感染或使机体内潜在的感染灶扩大或扩散,还可使原来静止的结核灶扩散。在用药过程中应注意病情的变化及是否有诱发感染现象,同时给予抗感染治疗。
3、 诱发或加重消化性溃疡:糖皮质激素除妨碍组织修复、延缓组织愈合外,还可使胃酸及胃蛋白酶分泌增多,又能减少胃粘液分泌,降低胃粘膜的抵抗力,可诱发或加重胃、十二指肠溃疡出血,甚至造成消化道穿孔。
4、 神经症状:可发生激动、失眠,个别病人可诱发精神病,癫痫病人可诱发癫痫发作。故有精神病倾向病人、精神病人及癫痫者应禁用。
5、肾上腺皮质萎缩或功能不全:较长期应用该类药物,由于体内糖皮质激素水平长期高于正常,可引起负反馈作用,而影响下丘脑及垂体前叶分泌促肾上腺皮质激素,使内源性糖皮质激素分泌减少或导致肾上腺皮质激素功能不全。一旦遇到应激时,如出血、感染,则可出现头晕、恶心、呕吐、低血压、低血糖或发生低血糖昏迷。
6、 反跳现象及停药症状:长期应用 激素类药物,症状基本控制时,若减量太大或突然停药,原来症状可很快出现或加重,此种现象称为反跳现象。这是因病人对激素产生依赖作用或症状尚未完全被控制所致。处理措施为恢复激素用量,待症状控制后再缓慢减量。
药物的相互作用
1、与降血钾药(如两性霉素B、排钾利尿药、刺激性泻药、洋地黄类)合用,增加低血钾的危险性。
2、与抗凝药合用可影响口服抗凝药的代谢以及凝血因子的作用,增加出血的危险性。
3、与胰岛素,二甲双胍、磺脲类降糖药合用时,可降低降血糖的作用,应调整降糖药的用量。
4、与镁、铝、钙的盐、氧化物及氢氧化物合用可降低曲安奈德的吸收。
5、与α-干扰素合用可能抑制干扰素的作用。
6、与乙酰水杨酸类合用可降低水杨酸的吸收,应调整水杨酸的使用剂量。
7、酶诱导剂可降低曲安奈德的疗效,与其合用时应调整曲安奈德的剂量。
编号 | 毒性类型 | 测试方法 | 测试对象 | 使用剂量 | 毒性作用 |
|---|---|---|---|---|---|
1 | 肌肉注射 | 成年男性 | 571 μg/kg | 血管毒性——休克 皮肤和附件毒性——皮炎 (全身暴露后) | |
2 | 急性毒性 | 肠外 | 成年女性 | 4 mg/kg | 行为毒性——肌肉无力 血管毒性——血压身高,不具有自主神经节 |
3 | 急性毒性 | 皮下注射 | 大鼠 | 13100 μg/kg | 详细作用没有报告除致死剂量以外的其他值 |
4 | 急性毒性 | 口服 | 5 mg/kg | 详细作用没有报告除致死剂量以外的其他值 | |
5 | 急性毒性 | 腹腔注射 | 小鼠 | 105 mg/kg | 详细作用没有报告除致死剂量以外的其他值 |
6 | 急性毒性 | 皮下注射 | 小鼠 | 132 mg/kg | 详细作用没有报告除致死剂量以外的其他值 |
7 | 突变毒性 | 人类 细胞 | 1 nmol/L | ||
8 | 突变毒性 | 人类 细胞 | 10 nmol/L | ||
9 | 突变毒性 | 皮肤表面 | 人类 | 5000 ppm | |
10 | 突变毒性 | 皮肤表面 | 人类 | 5000 ppm | |
11 | 突变毒性 | 小鼠 细胞 | 1 nmol/L | ||
12 | 突变毒性 | 小鼠白细胞 | 10 nmol/L | ||
13 | 生殖毒性 | 皮肤表面 | 成年女性 | 101 mg/kg 雌性受孕 12-29 周后 | 生殖毒性——胎儿毒性 (如胎儿发育不良,但不至死亡) 生殖毒性——胃肠道系统发育异常 |
14 | 生殖毒性 | 皮下注射 | 大鼠 | 450 μg/kg 雌性受孕 11-19 天后 | 生殖毒性——影响分娩 生殖毒性——胎儿毒性 (如胎儿发育不良,但不至死亡) 生殖毒性——新生儿体重增加量减少 |
15 | 生殖毒性 | 皮下注射 | 大鼠 | 900 mg/kg 雌性受孕 11-19 天后 | 生殖毒性——胚胎或胎儿死亡 |
16 | 生殖毒性 | 皮下注射 | 大鼠 | 1 mg/kg 雌性受孕 14-15 天后 | 生殖毒性——颅骨和面部发育异常 (包括鼻/舌) |
17 | 生殖毒性 | 皮下注射 | 大鼠 | 2 mg/kg 雌性受孕 14-15 天后 | 生殖毒性——植入后死亡率增加 |
18 | 生殖毒性 | 肌肉注射 | 大鼠 | 375 μg/kg 雌性受孕 12-14 天后 | 生殖毒性——胎儿毒性 (如胎儿发育不良,但不至死亡) |
19 | 生殖毒性 | 肌肉注射 | 大鼠 | 500 μg/kg 雌性受孕 14 天后 | 生殖毒性——颅骨和面部发育异常 (包括鼻/舌) 生殖毒性——影响胎儿 |
20 | 生殖毒性 | 肌肉注射 | 大鼠 | 750 μg/kg 雌性受孕 12-14 天后 | 生殖毒性——对新生儿有影响 |
21 | 生殖毒性 | 肌肉注射 | 大鼠 | 1500 μg/kg 雌性受孕 12-14 天后 | 生殖毒性——泌尿系统发育异常 |
22 | 生殖毒性 | 肌肉注射 | 大鼠 | 750 μg/kg 雌性受孕 12-14 天后 | 生殖毒性——植入后死亡率增加 生殖毒性——影响产仔数 生殖毒性——胚胎或胎儿死亡 |
23 | 生殖毒性 | 腹腔注射 | 小鼠 | 13 mg/kg 雌性受孕 12 天后 | 生殖毒性——影响胎儿 |
24 | 生殖毒性 | 皮下注射 | 小鼠 | 12800 μg/kg 雌性受孕 11-14 天后 | 生殖毒性——植入后死亡率增加 |
25 | 生殖毒性 | 皮下注射 | 小鼠 | 960 μg/kg 雌性受孕 11-14 天后 | 生殖毒性——颅骨和面部发育异常 (包括鼻/舌) |
26 | 生殖毒性 | 皮下注射 | 小鼠 | 2500 μg/kg 雌性受孕 12 天后 | 生殖毒性——植入后死亡率增加 生殖毒性——颅骨和面部发育异常 (包括鼻/舌) |
27 | 生殖毒性 | 皮下注射 | 小鼠 | 10 mg/kg 雌性受孕 11 天后 | 生殖毒性——胚胎或胎儿死亡 生殖毒性——颅骨和面部发育异常 (包括鼻/舌) |
28 | 生殖毒性 | 皮下注射 | 小鼠 | 12800 μg/kg 雌性受孕 11 天后 | 生殖毒性——胎儿毒性 (如胎儿发育不良,但不至死亡) |
29 | 生殖毒性 | 肌肉注射 | 小鼠 | 480 μg/kg 雌性受孕 11-14 天后 | 生殖毒性——颅骨和面部发育异常 (包括鼻/舌) |
30 | 生殖毒性 | 肌肉注射 | 小鼠 | 10 mg/kg 雌性受孕 11 天后 | 生殖毒性——影响胎儿 |
31 | 生殖毒性 | 肌肉注射 | 小鼠 | 5 mg/kg 雌性受孕 11 天后 | 生殖毒性——植入后死亡率增加 生殖毒性——颅骨和面部发育异常 (包括鼻/舌) |
32 | 生殖毒性 | 肌肉注射 | 小鼠 | 10 mg/kg 雌性受孕 11 天后 | 生殖毒性——影响胎儿或胚胎细胞遗传物质 |
33 | 生殖毒性 | 肌肉注射 | 小鼠 | 10 mg/kg 雌性受孕 11 天后 | 生殖毒性——胎儿毒性 (如胎儿发育不良,但不至死亡) 生殖毒性——胚胎或胎儿死亡 生殖毒性——颅骨和面部发育异常 (包括鼻/舌) |
34 | 生殖毒性 | 注入 | 小鼠 | 650 μg/kg 雌性受孕 6-18 天后 | 生殖毒性——胎儿毒性 (如胎儿发育不良,但不至死亡) |
35 | 生殖毒性 | 注入 | 小鼠 | 6500 μg/kg 雌性受孕 6-18 天后 | 生殖毒性——胚胎植入前死亡率上升 |
36 | 生殖毒性 | 肌肉注射 | 猴 | 50 mg/kg 雌性受孕 23-31 天后 | 生殖毒性——中枢神经系统发育异常 生殖毒性——耳/眼发育异常 生殖毒性——颅骨和面部发育异常 (包括鼻/舌) |
37 | 生殖毒性 | 肌肉注射 | 猴 | 60 mg/kg 雌性受孕 41-44 天后 | 生殖毒性——颅骨和面部发育异常 (包括鼻/舌) 生殖毒性——肌肉骨骼系统发育异常 生殖毒性——血液和淋巴系统发育异常 (包括脾和骨髓) |
38 | 生殖毒性 | 肌肉注射 | 猴 | 60 mg/kg 雌性受孕 41-44 天后 | 生殖毒性——胎儿毒性 (如胎儿发育不良,但不至死亡) 生殖毒性——胚胎或胎儿死亡 |
39 | 生殖毒性 | 肌肉注射 | 猴 | 50 mg/kg 雌性受孕 23-31 天后 | 生殖毒性——机体稳态发育异常 |
40 | 生殖毒性 | 肌肉注射 | 猴 | 3 mg/kg 雌性受孕 63-65 天后 | 生殖毒性——呼吸系统发育异常 |
41 | 生殖毒性 | 肌肉注射 | 仓鼠 | 500 μg/kg 雌性受孕 9 天后 | 生殖毒性——植入后死亡率增加 生殖毒性——中枢神经系统发育异常 生殖毒性——其他发育异常 |
42 | 生殖毒性 | 肌肉注射 | 仓鼠 | 100 μg/kg 雌性受孕 11 天后 | 生殖毒性——内分泌系统发育异常 生殖毒性——影响新生儿的生化和代谢 |
安全术语
S45:In case of accident or if you feel unwell, seek medical advice immediately (show the lable where possible).
发生事故时或感觉不适时,立即求医(可能时出示标签)。
S53:Avoid exposure - obtain special instruCTions before use.
避免接触,使用前获得特别指示说明。
风险术语
R61:May cause harm to the unborn child.
可能对未出生婴儿造成危害。
1、本站所有文本、信息、视频文件等,仅代表本站观点或作者本人观点,请网友谨慎参考使用。
2、本站信息均为作者提供和网友推荐收集整理而来,仅供学习和研究使用。
3、对任何由于使用本站内容而引起的诉讼、纠纷,本站不承担任何责任。
4、如有侵犯你版权的,请来信(邮箱:baike52199@gmail.com)指出,核实后,本站将立即删除。